Склад води та її будова
Однією з найважливіших хімічних сполук для людства є вода. Вода займає ¾ всієї поверхні Землі. Світові запаси води досить великі ≈ 1389 млн. км3, якщо їх розподілити порівну, то на кожного жителя планети припало би по 280 млрд. л. Однак 97% водних ресурсів: моря й океани, де вода дуже солона і всього 3% – прісна вода, але лише 0,003% можна використовувати, тому що вода або сильно забруднена, або знаходиться на великій глибині, або міститься в айсбергах, в атмосфері, в ґрунті.
БУДОВА ВОДИ
Між атомами Гідрогену (1s1) і атомами Оксигену 1s22s22р4 в молекулі води утворюється два ковалентних полярних зв’язки за обмінним механізмом:
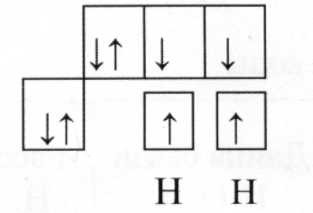
Атом Оксигену в молекулі води знаходиться в стані sр3 – гібридизації.
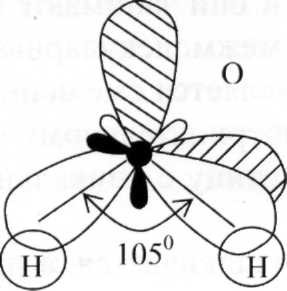
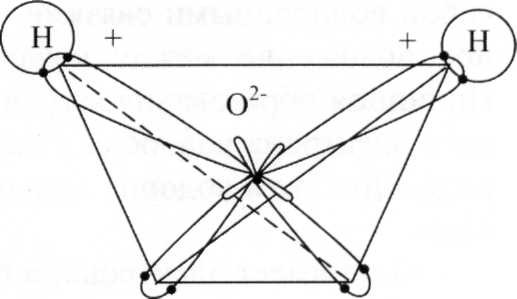
В молекулі води центри атомів Гідрогену та Оксигену утворюють рівнобедрений трикутник.
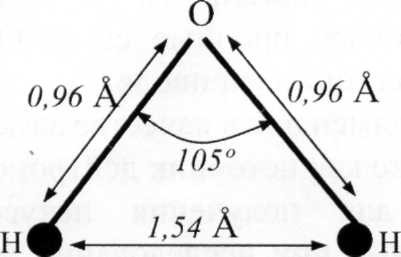
Вода має високу полярність (μ(Н2О)=1,85D), вода як хімічно активна сполука, зумовлює електролітичну дисоціацію солей, кислот, основ.
Молекули води не утворюють асоціатів у стані пару.
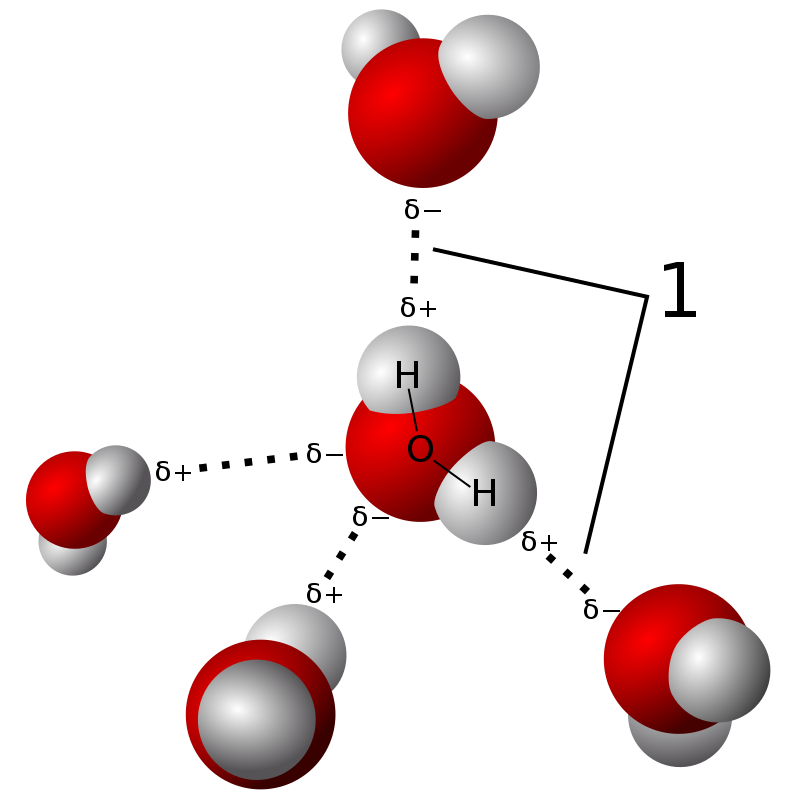
Молекули води з’єднані між собою водневими зв’язками. Енергія водневого зв’язку в воді дорівнює 29 кДж/моль. Водневі зв’язки об’єднують молекули води в асоціати, що є причиною аномально високих температур її кипіння та замерзання.
Водневі зв’язки впливають на розчинність речовин. У воді добре розчиняються речовини, що містять в складі полярні групи чи іонний зв'язок, наприклад, спирти, аміни, солі, кислоти, основи, гази (NH3, CO2, SO2) та інші. Вода здатна до донорно-акцепторної взаємодії, вона проявляє властивості донора за рахунок неподіленої пари електронів атома Оксисену, що і пояснює високу хімічну активність води та здатність її до комплексоутворення. Вода – слабкий електроліт, тому іонізує в незначній ступені:
Н2О … Н2О → Н3О+ + ОН-
чи спрощено:
Н2О ↔ Н+ + ОН-
К = [Н+] [ОН-]/[Н2О] = 1,86∙10-16
Агрегатні стани води (показані молекули)